Créer des répliques d’organes sur des puces de plastique pour accélérer les tests
C’est là que les organes sur puce entrent en jeu. Un organe sur puce est un système miniaturisé dans lequel sont creusés des canaux microfluidiques selon une architecture appropriée. Le squelette de ce système, typiquement de la taille d’une carte de crédit, est appelé « puce ». Cette puce permet de reproduire une fonctionnalité d’un organe, par exemple la respiration au niveau des alvéoles pulmonaires. La mise en culture des cellules se fait dans les canaux microfluidiques qui peuvent être compartimentés afin d’accueillir différents types de cellules, d’où la dénomination d’« organe sur puce ». La microfluidique permet d’entretenir les cellules en laissant s’écouler le milieu de culture (qui délivre aux cellules tous les nutriments dont elles ont besoin) durant plusieurs semaines.
Les organes sur puce sont ainsi la résultante d’un lien inextricable entre une partie puce, gouvernée par la microfluidique, et une partie biologie. En proposant des architectures tridimensionnelles et dynamiques, plus proches de la réalité humaine que les standards 2D, ils surpassent les modèles classiques in vitro. Grâce à l’utilisation de cellules humaines, ils devancent le modèle animal. Ces organes sur puce pourraient ainsi se substituer aux tests précliniques et détecter l’inefficacité ou la toxicité sur l’homme de certains composés sans avoir recours à des phases d’essais cliniques : ce serait un gain de temps et d’argent.
Au-delà des atouts économiques évidents, les organes sur puce offrent d’autres perspectives. D’abord, ils constituent un excellent modèle pour la recherche fondamentale. La puce, faite d’un matériau transparent – silicone ou plastique – peut être observée au microscope. Les différents mécanismes biologiques modélisés dans les canaux microfluidiques peuvent ainsi être étudiés dans une configuration aussi représentative que possible du corps humain, y compris avec des cellules modèles de différentes pathologies, par exemple des cellules portant une mutation du gène CFTR, propre aux cellules de patients atteints de la mucoviscidose.
Nombre d’organes ont été étudiés au cours des dernières années. Aujourd’hui, des recherches visant à améliorer notre compréhension du corps humain sont menées sur des intestins sur puce, des pancréas sur puce, des cœurs sur puce ou encore des cerveaux sur puce. On peut aussi par exemple développer un système vasculaire sur puce afin de mieux comprendre la formation des vaisseaux sanguins, qui joue un rôle essentiel dans le développement des cancers.
Vers une médecine personnalisée
Voyons plus loin encore. S’il est possible d’étudier dans une puce microfluidique des cellules humaines, pourquoi ne pas focaliser l’étude sur un groupe de personnes donné ? En faisant s’écouler différents médicaments dans la puce, des tests thérapeutiques pourraient être réalisés sur des cellules de femmes enceintes, d’enfants ou de toute autre population dont on souhaiterait connaître la réponse physiologique spécifique. Cette alternative est même parfois la seule façon de procéder. Par exemple, lorsqu’il s’agit d’étudier l’impact des radiations sur l’homme, mieux vaut que les essais soient réalisés sur des cellules déportées dans une puce !
Poussons désormais ce concept à l’extrême. S’il est possible d’étudier dans une puce microfluidique les cellules d’une population donnée, on pourrait envisager d’étudier les cellules et organes sur puce correspondant à un individu en particulier. C’est le but visé par la médecine personnalisée. Chaque patient pourrait ainsi bénéficier d’un traitement adapté à ses maux, dont l’efficacité aurait été préalablement évaluée dans « son » organe sur puce. Nous sommes en effet tous génétiquement différents, et la réponse au même médicament peut-être très variable dans la population. Ainsi en moyenne, seulement un patient sur trois répond au traitement anticancéreux qui lui est proposé. Disposer d’organes sur puce individualisés, qui contiendraient par exemple les cellules cancéreuses des patients à soigner, permettrait de tester rapidement une multitude de traitements afin de savoir lequel est le plus efficace pour combattre la tumeur d’un patient donné.
Toutefois, il demeure encore bien des défis à relever avant que les organes sur puce s’imposent chez les industriels et dans les hôpitaux. Il faut encore confirmer sur le plan scientifique leur pertinence par rapport aux modèles animaux employés à l’heure actuelle. De plus, les organes sur puce et la microfluidique en général sont encore trop souvent difficiles d’utilisation. Des efforts doivent être faits pour simplifier l’instrumentation de tels systèmes afin de proposer, au personnel hospitalier par exemple, des outils plus simples d’utilisation.
Yves Fouillet, du Laboratoire des systèmes microfluidiques et bio-ingénierie du CEA Grenoble, explique : « Les outils microfluidiques sont parfaitement adaptés à la problématique, mais il est nécessaire de les repenser pour répondre aux contraintes d’utilisation de la culture cellulaire. L’enjeu est de faciliter la dissémination des organes sur puce dans différents laboratoires, académiques ou non ». Bien qu’un gros travail pour la simplification des systèmes microfluidiques reste à mener, il est satisfaisant d’observer l’émergence de nombreuses entreprises liées aux organes sur puce ces dernières années. Le marché des organes sur puce, en augmentation de 70 % par rapport à 2015, laisse présager un avenir radieux pour les industriels. Le Wyss Institute, institut de recherche rattaché à l’université Harvard et pionnier dans le domaine des organes sur puce, fut lui-même fondé sur la devise suivante : « Une grande découverte ne peut pas changer le monde si elle ne sort pas du labo ».![]()
Clément Quintard, Doctorant en microfluidique pour applications biomédicales, CEA-Leti, Grenoble, Commissariat à l’énergie atomique et aux énergies alternatives (CEA)
Cet article est republié à partir de The Conversation sous licence Creative Commons. Lire l’article original.
Les organes sur puce : vers une médecine personnalisable

Nous sommes actuellement confrontés à un défi mondial pour la santé : la façon dont nous découvrons et développons de nouveaux médicaments est trop coûteuse et trop longue. Les organes sur puce pourraient permettre de répondre à ces difficultés et pourraient à l’avenir ouvrir la possibilité de faire des tests personnalisés pour chaque individu.
Le développement de médicaments : un enjeu de santé mondial
L’engouement des dernières années pour les organes sur puce réside dans une inquiétante réalité : le modèle de développement de nouveaux médicaments est dans une impasse. Cela signifie que des patients qui ont besoin de nouvelles thérapies ne les reçoivent pas et que des maladies ne sont pas traitées. Les chercheurs ont décrit ironiquement cette situation par une loi baptisée loi d’Eroom (Moore écrit à l’envers) stipulant que le développement d’un nouveau médicament est de plus en plus cher et de plus en plus long au fil du temps.
« Aujourd’hui, l’industrie pharmaceutique est face à un modèle qui ne fonctionne plus car pour dix mille molécules testées, une seule finira chez le patient, notamment à cause de l’inadéquation des modèles utilisés »
Xavier Gidrol, directeur du laboratoire Biomics au CEA Grenoble.
Chaque molécule candidate doit en effet suivre un long parcours en vue d’être approuvée sur le marché. Bien qu’une efficacité de la molécule puisse être décelée lors des premiers tests sur des cultures 2D in vitro et sur des animaux, ces modèles éloignés de la réalité physiologique du corps humain ne prédisent que très mal l’efficacité de la molécule sur l’homme.
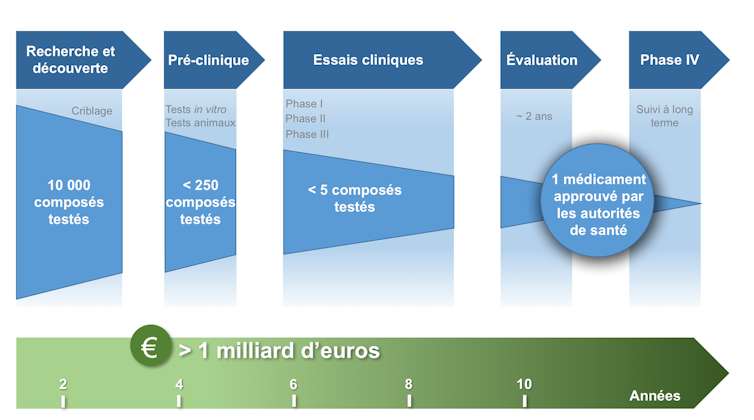
Se dresse alors un mur quasi infranchissable : les phases d’essais cliniques sur les humains. Ce sont ces phases d’essai très longues et très coûteuses qui mettent à mal les entreprises pharmaceutiques, qui, n’osant rêver de résultats spectaculaires, adoptent le sinistre mantra : « échouer plus vite et moins cher ».
Créer des répliques d’organes sur des puces de plastique pour accélérer les tests
C’est là que les organes sur puce entrent en jeu. Un organe sur puce est un système miniaturisé dans lequel sont creusés des canaux microfluidiques selon une architecture appropriée. Le squelette de ce système, typiquement de la taille d’une carte de crédit, est appelé « puce ». Cette puce permet de reproduire une fonctionnalité d’un organe, par exemple la respiration au niveau des alvéoles pulmonaires. La mise en culture des cellules se fait dans les canaux microfluidiques qui peuvent être compartimentés afin d’accueillir différents types de cellules, d’où la dénomination d’« organe sur puce ». La microfluidique permet d’entretenir les cellules en laissant s’écouler le milieu de culture (qui délivre aux cellules tous les nutriments dont elles ont besoin) durant plusieurs semaines.
Les organes sur puce sont ainsi la résultante d’un lien inextricable entre une partie puce, gouvernée par la microfluidique, et une partie biologie. En proposant des architectures tridimensionnelles et dynamiques, plus proches de la réalité humaine que les standards 2D, ils surpassent les modèles classiques in vitro. Grâce à l’utilisation de cellules humaines, ils devancent le modèle animal. Ces organes sur puce pourraient ainsi se substituer aux tests précliniques et détecter l’inefficacité ou la toxicité sur l’homme de certains composés sans avoir recours à des phases d’essais cliniques : ce serait un gain de temps et d’argent.
Au-delà des atouts économiques évidents, les organes sur puce offrent d’autres perspectives. D’abord, ils constituent un excellent modèle pour la recherche fondamentale. La puce, faite d’un matériau transparent – silicone ou plastique – peut être observée au microscope. Les différents mécanismes biologiques modélisés dans les canaux microfluidiques peuvent ainsi être étudiés dans une configuration aussi représentative que possible du corps humain, y compris avec des cellules modèles de différentes pathologies, par exemple des cellules portant une mutation du gène CFTR, propre aux cellules de patients atteints de la mucoviscidose.
Nombre d’organes ont été étudiés au cours des dernières années. Aujourd’hui, des recherches visant à améliorer notre compréhension du corps humain sont menées sur des intestins sur puce, des pancréas sur puce, des cœurs sur puce ou encore des cerveaux sur puce. On peut aussi par exemple développer un système vasculaire sur puce afin de mieux comprendre la formation des vaisseaux sanguins, qui joue un rôle essentiel dans le développement des cancers.
Vers une médecine personnalisée
Voyons plus loin encore. S’il est possible d’étudier dans une puce microfluidique des cellules humaines, pourquoi ne pas focaliser l’étude sur un groupe de personnes donné ? En faisant s’écouler différents médicaments dans la puce, des tests thérapeutiques pourraient être réalisés sur des cellules de femmes enceintes, d’enfants ou de toute autre population dont on souhaiterait connaître la réponse physiologique spécifique. Cette alternative est même parfois la seule façon de procéder. Par exemple, lorsqu’il s’agit d’étudier l’impact des radiations sur l’homme, mieux vaut que les essais soient réalisés sur des cellules déportées dans une puce !
Poussons désormais ce concept à l’extrême. S’il est possible d’étudier dans une puce microfluidique les cellules d’une population donnée, on pourrait envisager d’étudier les cellules et organes sur puce correspondant à un individu en particulier. C’est le but visé par la médecine personnalisée. Chaque patient pourrait ainsi bénéficier d’un traitement adapté à ses maux, dont l’efficacité aurait été préalablement évaluée dans « son » organe sur puce. Nous sommes en effet tous génétiquement différents, et la réponse au même médicament peut-être très variable dans la population. Ainsi en moyenne, seulement un patient sur trois répond au traitement anticancéreux qui lui est proposé. Disposer d’organes sur puce individualisés, qui contiendraient par exemple les cellules cancéreuses des patients à soigner, permettrait de tester rapidement une multitude de traitements afin de savoir lequel est le plus efficace pour combattre la tumeur d’un patient donné.
Toutefois, il demeure encore bien des défis à relever avant que les organes sur puce s’imposent chez les industriels et dans les hôpitaux. Il faut encore confirmer sur le plan scientifique leur pertinence par rapport aux modèles animaux employés à l’heure actuelle. De plus, les organes sur puce et la microfluidique en général sont encore trop souvent difficiles d’utilisation. Des efforts doivent être faits pour simplifier l’instrumentation de tels systèmes afin de proposer, au personnel hospitalier par exemple, des outils plus simples d’utilisation.
Yves Fouillet, du Laboratoire des systèmes microfluidiques et bio-ingénierie du CEA Grenoble, explique : « Les outils microfluidiques sont parfaitement adaptés à la problématique, mais il est nécessaire de les repenser pour répondre aux contraintes d’utilisation de la culture cellulaire. L’enjeu est de faciliter la dissémination des organes sur puce dans différents laboratoires, académiques ou non ». Bien qu’un gros travail pour la simplification des systèmes microfluidiques reste à mener, il est satisfaisant d’observer l’émergence de nombreuses entreprises liées aux organes sur puce ces dernières années. Le marché des organes sur puce, en augmentation de 70 % par rapport à 2015, laisse présager un avenir radieux pour les industriels. Le Wyss Institute, institut de recherche rattaché à l’université Harvard et pionnier dans le domaine des organes sur puce, fut lui-même fondé sur la devise suivante : « Une grande découverte ne peut pas changer le monde si elle ne sort pas du labo ».![]()
Clément Quintard, Doctorant en microfluidique pour applications biomédicales, CEA-Leti, Grenoble, Commissariat à l’énergie atomique et aux énergies alternatives (CEA)
Cet article est republié à partir de The Conversation sous licence Creative Commons. Lire l’article original.
Towards Personalized Medicine
Looking further, if it’s possible to study human cells in a microfluidic chip, why not focus on a specific group of people? By flowing different drugs through the chip, therapeutic tests could be conducted on cells from pregnant women, children, or any other population whose specific physiological response we’d like to understand. This alternative is sometimes the only way to proceed. For example, when studying the impact of radiation on humans, it’s better for tests to be conducted on cells placed in a chip!
Pushing this concept to the extreme, if it’s possible to study cells from a specific population in a microfluidic chip, we could consider studying cells and organs on a chip corresponding to a particular individual. This is the goal of personalized medicine. Each patient could benefit from a treatment tailored to their ailments, with its effectiveness previously evaluated in “their” organ on a chip. We are all genetically different, and the response to the same drug can vary significantly in the population. On average, only one in three patients responds to the proposed cancer treatment. Having individualized organs on chips, which would contain, for example, the cancer cells of the patients to be treated, would allow for the quick testing of multiple treatments to determine which is most effective in combating a given patient’s tumor.
However, many challenges remain before organs on chips become standard in industries and hospitals. Their relevance compared to currently used animal models still needs scientific confirmation. Moreover, organs on chips and microfluidics, in general, are often too complicated to use. Efforts must be made to simplify the instrumentation of such systems to offer hospital staff, for instance, simpler tools.
Yves Fouillet, from the Laboratory of Microfluidic Systems and Bioengineering at CEA Grenoble, explains, “Microfluidic tools are perfectly suited to the problem, but they need to be rethought to meet the constraints of cell culture use. The challenge is to facilitate the dissemination of organs on chips in various laboratories, academic or not.” Although significant work remains in simplifying microfluidic systems, it’s encouraging to see the emergence of many companies related to organs on chips in recent years. The market for organs on chips, up 70% compared to 2015, suggests a bright future for the industry. The Wyss Institute, a research institute affiliated with Harvard University and a pioneer in the field of organs on chips, was founded on the following motto: “Discoveries can’t change the world if they don’t leave the lab.”
Les organes sur puce : vers une médecine personnalisable

Nous sommes actuellement confrontés à un défi mondial pour la santé : la façon dont nous découvrons et développons de nouveaux médicaments est trop coûteuse et trop longue. Les organes sur puce pourraient permettre de répondre à ces difficultés et pourraient à l’avenir ouvrir la possibilité de faire des tests personnalisés pour chaque individu.
Le développement de médicaments : un enjeu de santé mondial
L’engouement des dernières années pour les organes sur puce réside dans une inquiétante réalité : le modèle de développement de nouveaux médicaments est dans une impasse. Cela signifie que des patients qui ont besoin de nouvelles thérapies ne les reçoivent pas et que des maladies ne sont pas traitées. Les chercheurs ont décrit ironiquement cette situation par une loi baptisée loi d’Eroom (Moore écrit à l’envers) stipulant que le développement d’un nouveau médicament est de plus en plus cher et de plus en plus long au fil du temps.
« Aujourd’hui, l’industrie pharmaceutique est face à un modèle qui ne fonctionne plus car pour dix mille molécules testées, une seule finira chez le patient, notamment à cause de l’inadéquation des modèles utilisés »
Xavier Gidrol, directeur du laboratoire Biomics au CEA Grenoble.
Chaque molécule candidate doit en effet suivre un long parcours en vue d’être approuvée sur le marché. Bien qu’une efficacité de la molécule puisse être décelée lors des premiers tests sur des cultures 2D in vitro et sur des animaux, ces modèles éloignés de la réalité physiologique du corps humain ne prédisent que très mal l’efficacité de la molécule sur l’homme.

Se dresse alors un mur quasi infranchissable : les phases d’essais cliniques sur les humains. Ce sont ces phases d’essai très longues et très coûteuses qui mettent à mal les entreprises pharmaceutiques, qui, n’osant rêver de résultats spectaculaires, adoptent le sinistre mantra : « échouer plus vite et moins cher ».
Créer des répliques d’organes sur des puces de plastique pour accélérer les tests
C’est là que les organes sur puce entrent en jeu. Un organe sur puce est un système miniaturisé dans lequel sont creusés des canaux microfluidiques selon une architecture appropriée. Le squelette de ce système, typiquement de la taille d’une carte de crédit, est appelé « puce ». Cette puce permet de reproduire une fonctionnalité d’un organe, par exemple la respiration au niveau des alvéoles pulmonaires. La mise en culture des cellules se fait dans les canaux microfluidiques qui peuvent être compartimentés afin d’accueillir différents types de cellules, d’où la dénomination d’« organe sur puce ». La microfluidique permet d’entretenir les cellules en laissant s’écouler le milieu de culture (qui délivre aux cellules tous les nutriments dont elles ont besoin) durant plusieurs semaines.
Les organes sur puce sont ainsi la résultante d’un lien inextricable entre une partie puce, gouvernée par la microfluidique, et une partie biologie. En proposant des architectures tridimensionnelles et dynamiques, plus proches de la réalité humaine que les standards 2D, ils surpassent les modèles classiques in vitro. Grâce à l’utilisation de cellules humaines, ils devancent le modèle animal. Ces organes sur puce pourraient ainsi se substituer aux tests précliniques et détecter l’inefficacité ou la toxicité sur l’homme de certains composés sans avoir recours à des phases d’essais cliniques : ce serait un gain de temps et d’argent.
Au-delà des atouts économiques évidents, les organes sur puce offrent d’autres perspectives. D’abord, ils constituent un excellent modèle pour la recherche fondamentale. La puce, faite d’un matériau transparent – silicone ou plastique – peut être observée au microscope. Les différents mécanismes biologiques modélisés dans les canaux microfluidiques peuvent ainsi être étudiés dans une configuration aussi représentative que possible du corps humain, y compris avec des cellules modèles de différentes pathologies, par exemple des cellules portant une mutation du gène CFTR, propre aux cellules de patients atteints de la mucoviscidose.
Nombre d’organes ont été étudiés au cours des dernières années. Aujourd’hui, des recherches visant à améliorer notre compréhension du corps humain sont menées sur des intestins sur puce, des pancréas sur puce, des cœurs sur puce ou encore des cerveaux sur puce. On peut aussi par exemple développer un système vasculaire sur puce afin de mieux comprendre la formation des vaisseaux sanguins, qui joue un rôle essentiel dans le développement des cancers.
Vers une médecine personnalisée
Voyons plus loin encore. S’il est possible d’étudier dans une puce microfluidique des cellules humaines, pourquoi ne pas focaliser l’étude sur un groupe de personnes donné ? En faisant s’écouler différents médicaments dans la puce, des tests thérapeutiques pourraient être réalisés sur des cellules de femmes enceintes, d’enfants ou de toute autre population dont on souhaiterait connaître la réponse physiologique spécifique. Cette alternative est même parfois la seule façon de procéder. Par exemple, lorsqu’il s’agit d’étudier l’impact des radiations sur l’homme, mieux vaut que les essais soient réalisés sur des cellules déportées dans une puce !
Poussons désormais ce concept à l’extrême. S’il est possible d’étudier dans une puce microfluidique les cellules d’une population donnée, on pourrait envisager d’étudier les cellules et organes sur puce correspondant à un individu en particulier. C’est le but visé par la médecine personnalisée. Chaque patient pourrait ainsi bénéficier d’un traitement adapté à ses maux, dont l’efficacité aurait été préalablement évaluée dans « son » organe sur puce. Nous sommes en effet tous génétiquement différents, et la réponse au même médicament peut-être très variable dans la population. Ainsi en moyenne, seulement un patient sur trois répond au traitement anticancéreux qui lui est proposé. Disposer d’organes sur puce individualisés, qui contiendraient par exemple les cellules cancéreuses des patients à soigner, permettrait de tester rapidement une multitude de traitements afin de savoir lequel est le plus efficace pour combattre la tumeur d’un patient donné.
Toutefois, il demeure encore bien des défis à relever avant que les organes sur puce s’imposent chez les industriels et dans les hôpitaux. Il faut encore confirmer sur le plan scientifique leur pertinence par rapport aux modèles animaux employés à l’heure actuelle. De plus, les organes sur puce et la microfluidique en général sont encore trop souvent difficiles d’utilisation. Des efforts doivent être faits pour simplifier l’instrumentation de tels systèmes afin de proposer, au personnel hospitalier par exemple, des outils plus simples d’utilisation.
Yves Fouillet, du Laboratoire des systèmes microfluidiques et bio-ingénierie du CEA Grenoble, explique : « Les outils microfluidiques sont parfaitement adaptés à la problématique, mais il est nécessaire de les repenser pour répondre aux contraintes d’utilisation de la culture cellulaire. L’enjeu est de faciliter la dissémination des organes sur puce dans différents laboratoires, académiques ou non ». Bien qu’un gros travail pour la simplification des systèmes microfluidiques reste à mener, il est satisfaisant d’observer l’émergence de nombreuses entreprises liées aux organes sur puce ces dernières années. Le marché des organes sur puce, en augmentation de 70 % par rapport à 2015, laisse présager un avenir radieux pour les industriels. Le Wyss Institute, institut de recherche rattaché à l’université Harvard et pionnier dans le domaine des organes sur puce, fut lui-même fondé sur la devise suivante : « Une grande découverte ne peut pas changer le monde si elle ne sort pas du labo ».![]()
Clément Quintard, Doctorant en microfluidique pour applications biomédicales, CEA-Leti, Grenoble, Commissariat à l’énergie atomique et aux énergies alternatives (CEA)
Cet article est republié à partir de The Conversation sous licence Creative Commons. Lire l’article original.
We are currently facing a global health challenge: the way we discover and develop new drugs is too costly and too lengthy. Organs on chips could address these challenges and may, in the future, offer the possibility of personalized testing for each individual.
→This article was published online for the media outlet The Conversation ←
Drug Development: A Global Health Issue
The recent enthusiasm for organs on chips stems from a concerning reality: the current model for new drug development is at a standstill. This means that patients in need of new therapies are not receiving them, and certain diseases remain untreated. Researchers have ironically described this situation with a law named Eroom’s law (Moore spelled backward), stating that the development of a new drug becomes increasingly expensive and lengthy over time.
Today, the pharmaceutical industry faces a model that no longer works because, for every ten thousand molecules tested, only one will end up with the patient, mainly due to the inadequacy of the models used.
Xavier Gidrol, director of the Biomics laboratory at CEA Grenoble.
Indeed, each candidate molecule must undergo a lengthy process to be approved for the market. Although a molecule’s effectiveness can be detected during initial tests on 2D in vitro cultures and animals, these models, distant from the physiological reality of the human body, poorly predict the molecule’s effectiveness in humans.
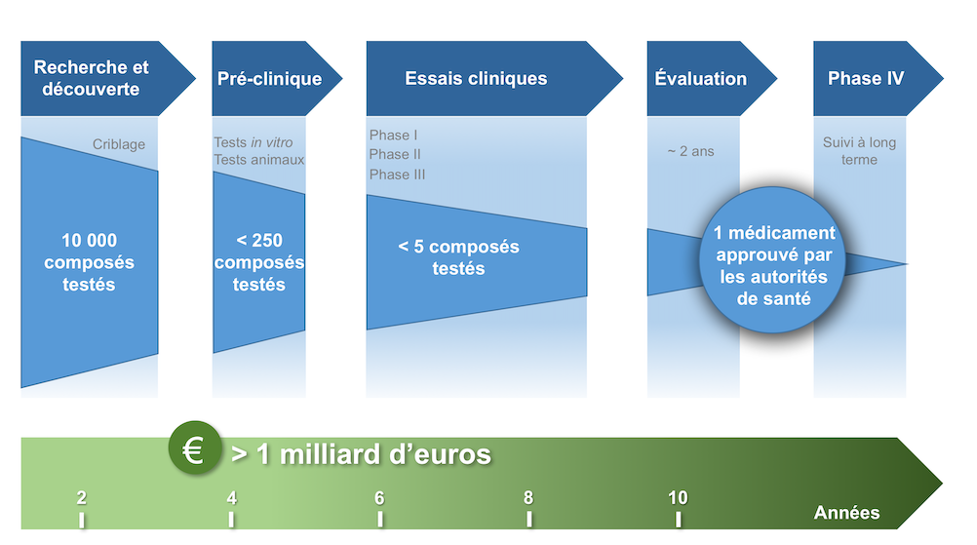
A nearly insurmountable wall then arises: the phases of clinical trials on humans. It is these lengthy and costly trial phases that challenge pharmaceutical companies, which, not daring to dream of spectacular results, adopt the grim mantra: “fail faster, fail cheaper.”
Creating Organ Replicas on Plastic Chips to Accelerate Testing
This is where organs on chips come into play. An organ on a chip is a miniaturized system in which microfluidic channels are carved according to an appropriate architecture. The framework of this system, typically the size of a credit card, is called a “chip.” This chip can replicate an organ’s functionality, for instance, respiration at the level of pulmonary alveoli. Cells are cultured within these microfluidic channels, which can be compartmentalized to accommodate different cell types, hence the term “organ on a chip.” Microfluidics allows the maintenance of cells by letting the culture medium (which provides cells with all the nutrients they need) flow for several weeks.
Organs on chips are thus the result of an inextricable link between a chip part, governed by microfluidics, and a biology part. By offering three-dimensional and dynamic architectures, closer to human reality than 2D standards, they surpass traditional in vitro models. Using human cells, they outpace animal models. These organs on chips could replace preclinical tests and detect the inefficiency or toxicity in humans of certain compounds without resorting to clinical trial phases: this would be a time and money saver.
Beyond the evident economic benefits, organs on chips offer other prospects. Firstly, they serve as an excellent model for fundamental research. The chip, made of a transparent material – silicone or plastic – can be observed under a microscope. Various biological mechanisms modeled in the microfluidic channels can thus be studied in a configuration as representative as possible of the human body, including with model cells of different pathologies, for instance, cells carrying a CFTR gene mutation, specific to cells of cystic fibrosis patients.
Numerous organs have been studied over recent years. Today, research aiming to improve our understanding of the human body is conducted on intestines on chips, pancreases on chips, hearts on chips, and even brains on chips. For instance, a vascular system on a chip can be developed to better understand blood vessel formation, which plays a crucial role in cancer development.
Towards Personalized Medicine
Looking further, if it’s possible to study human cells in a microfluidic chip, why not focus on a specific group of people? By flowing different drugs through the chip, therapeutic tests could be conducted on cells from pregnant women, children, or any other population whose specific physiological response we’d like to understand. This alternative is sometimes the only way to proceed. For example, when studying the impact of radiation on humans, it’s better for tests to be conducted on cells placed in a chip!
Pushing this concept to the extreme, if it’s possible to study cells from a specific population in a microfluidic chip, we could consider studying cells and organs on a chip corresponding to a particular individual. This is the goal of personalized medicine. Each patient could benefit from a treatment tailored to their ailments, with its effectiveness previously evaluated in “their” organ on a chip. We are all genetically different, and the response to the same drug can vary significantly in the population. On average, only one in three patients responds to the proposed cancer treatment. Having individualized organs on chips, which would contain, for example, the cancer cells of the patients to be treated, would allow for the quick testing of multiple treatments to determine which is most effective in combating a given patient’s tumor.
However, many challenges remain before organs on chips become standard in industries and hospitals. Their relevance compared to currently used animal models still needs scientific confirmation. Moreover, organs on chips and microfluidics, in general, are often too complicated to use. Efforts must be made to simplify the instrumentation of such systems to offer hospital staff, for instance, simpler tools.
Yves Fouillet, from the Laboratory of Microfluidic Systems and Bioengineering at CEA Grenoble, explains, “Microfluidic tools are perfectly suited to the problem, but they need to be rethought to meet the constraints of cell culture use. The challenge is to facilitate the dissemination of organs on chips in various laboratories, academic or not.” Although significant work remains in simplifying microfluidic systems, it’s encouraging to see the emergence of many companies related to organs on chips in recent years. The market for organs on chips, up 70% compared to 2015, suggests a bright future for the industry. The Wyss Institute, a research institute affiliated with Harvard University and a pioneer in the field of organs on chips, was founded on the following motto: “Discoveries can’t change the world if they don’t leave the lab.”
Les organes sur puce : vers une médecine personnalisable

Nous sommes actuellement confrontés à un défi mondial pour la santé : la façon dont nous découvrons et développons de nouveaux médicaments est trop coûteuse et trop longue. Les organes sur puce pourraient permettre de répondre à ces difficultés et pourraient à l’avenir ouvrir la possibilité de faire des tests personnalisés pour chaque individu.
Le développement de médicaments : un enjeu de santé mondial
L’engouement des dernières années pour les organes sur puce réside dans une inquiétante réalité : le modèle de développement de nouveaux médicaments est dans une impasse. Cela signifie que des patients qui ont besoin de nouvelles thérapies ne les reçoivent pas et que des maladies ne sont pas traitées. Les chercheurs ont décrit ironiquement cette situation par une loi baptisée loi d’Eroom (Moore écrit à l’envers) stipulant que le développement d’un nouveau médicament est de plus en plus cher et de plus en plus long au fil du temps.
« Aujourd’hui, l’industrie pharmaceutique est face à un modèle qui ne fonctionne plus car pour dix mille molécules testées, une seule finira chez le patient, notamment à cause de l’inadéquation des modèles utilisés »
Xavier Gidrol, directeur du laboratoire Biomics au CEA Grenoble.
Chaque molécule candidate doit en effet suivre un long parcours en vue d’être approuvée sur le marché. Bien qu’une efficacité de la molécule puisse être décelée lors des premiers tests sur des cultures 2D in vitro et sur des animaux, ces modèles éloignés de la réalité physiologique du corps humain ne prédisent que très mal l’efficacité de la molécule sur l’homme.

Se dresse alors un mur quasi infranchissable : les phases d’essais cliniques sur les humains. Ce sont ces phases d’essai très longues et très coûteuses qui mettent à mal les entreprises pharmaceutiques, qui, n’osant rêver de résultats spectaculaires, adoptent le sinistre mantra : « échouer plus vite et moins cher ».
Créer des répliques d’organes sur des puces de plastique pour accélérer les tests
C’est là que les organes sur puce entrent en jeu. Un organe sur puce est un système miniaturisé dans lequel sont creusés des canaux microfluidiques selon une architecture appropriée. Le squelette de ce système, typiquement de la taille d’une carte de crédit, est appelé « puce ». Cette puce permet de reproduire une fonctionnalité d’un organe, par exemple la respiration au niveau des alvéoles pulmonaires. La mise en culture des cellules se fait dans les canaux microfluidiques qui peuvent être compartimentés afin d’accueillir différents types de cellules, d’où la dénomination d’« organe sur puce ». La microfluidique permet d’entretenir les cellules en laissant s’écouler le milieu de culture (qui délivre aux cellules tous les nutriments dont elles ont besoin) durant plusieurs semaines.
Les organes sur puce sont ainsi la résultante d’un lien inextricable entre une partie puce, gouvernée par la microfluidique, et une partie biologie. En proposant des architectures tridimensionnelles et dynamiques, plus proches de la réalité humaine que les standards 2D, ils surpassent les modèles classiques in vitro. Grâce à l’utilisation de cellules humaines, ils devancent le modèle animal. Ces organes sur puce pourraient ainsi se substituer aux tests précliniques et détecter l’inefficacité ou la toxicité sur l’homme de certains composés sans avoir recours à des phases d’essais cliniques : ce serait un gain de temps et d’argent.
Au-delà des atouts économiques évidents, les organes sur puce offrent d’autres perspectives. D’abord, ils constituent un excellent modèle pour la recherche fondamentale. La puce, faite d’un matériau transparent – silicone ou plastique – peut être observée au microscope. Les différents mécanismes biologiques modélisés dans les canaux microfluidiques peuvent ainsi être étudiés dans une configuration aussi représentative que possible du corps humain, y compris avec des cellules modèles de différentes pathologies, par exemple des cellules portant une mutation du gène CFTR, propre aux cellules de patients atteints de la mucoviscidose.
Nombre d’organes ont été étudiés au cours des dernières années. Aujourd’hui, des recherches visant à améliorer notre compréhension du corps humain sont menées sur des intestins sur puce, des pancréas sur puce, des cœurs sur puce ou encore des cerveaux sur puce. On peut aussi par exemple développer un système vasculaire sur puce afin de mieux comprendre la formation des vaisseaux sanguins, qui joue un rôle essentiel dans le développement des cancers.
Vers une médecine personnalisée
Voyons plus loin encore. S’il est possible d’étudier dans une puce microfluidique des cellules humaines, pourquoi ne pas focaliser l’étude sur un groupe de personnes donné ? En faisant s’écouler différents médicaments dans la puce, des tests thérapeutiques pourraient être réalisés sur des cellules de femmes enceintes, d’enfants ou de toute autre population dont on souhaiterait connaître la réponse physiologique spécifique. Cette alternative est même parfois la seule façon de procéder. Par exemple, lorsqu’il s’agit d’étudier l’impact des radiations sur l’homme, mieux vaut que les essais soient réalisés sur des cellules déportées dans une puce !
Poussons désormais ce concept à l’extrême. S’il est possible d’étudier dans une puce microfluidique les cellules d’une population donnée, on pourrait envisager d’étudier les cellules et organes sur puce correspondant à un individu en particulier. C’est le but visé par la médecine personnalisée. Chaque patient pourrait ainsi bénéficier d’un traitement adapté à ses maux, dont l’efficacité aurait été préalablement évaluée dans « son » organe sur puce. Nous sommes en effet tous génétiquement différents, et la réponse au même médicament peut-être très variable dans la population. Ainsi en moyenne, seulement un patient sur trois répond au traitement anticancéreux qui lui est proposé. Disposer d’organes sur puce individualisés, qui contiendraient par exemple les cellules cancéreuses des patients à soigner, permettrait de tester rapidement une multitude de traitements afin de savoir lequel est le plus efficace pour combattre la tumeur d’un patient donné.
Toutefois, il demeure encore bien des défis à relever avant que les organes sur puce s’imposent chez les industriels et dans les hôpitaux. Il faut encore confirmer sur le plan scientifique leur pertinence par rapport aux modèles animaux employés à l’heure actuelle. De plus, les organes sur puce et la microfluidique en général sont encore trop souvent difficiles d’utilisation. Des efforts doivent être faits pour simplifier l’instrumentation de tels systèmes afin de proposer, au personnel hospitalier par exemple, des outils plus simples d’utilisation.
Yves Fouillet, du Laboratoire des systèmes microfluidiques et bio-ingénierie du CEA Grenoble, explique : « Les outils microfluidiques sont parfaitement adaptés à la problématique, mais il est nécessaire de les repenser pour répondre aux contraintes d’utilisation de la culture cellulaire. L’enjeu est de faciliter la dissémination des organes sur puce dans différents laboratoires, académiques ou non ». Bien qu’un gros travail pour la simplification des systèmes microfluidiques reste à mener, il est satisfaisant d’observer l’émergence de nombreuses entreprises liées aux organes sur puce ces dernières années. Le marché des organes sur puce, en augmentation de 70 % par rapport à 2015, laisse présager un avenir radieux pour les industriels. Le Wyss Institute, institut de recherche rattaché à l’université Harvard et pionnier dans le domaine des organes sur puce, fut lui-même fondé sur la devise suivante : « Une grande découverte ne peut pas changer le monde si elle ne sort pas du labo ».![]()
Clément Quintard, Doctorant en microfluidique pour applications biomédicales, CEA-Leti, Grenoble, Commissariat à l’énergie atomique et aux énergies alternatives (CEA)
Cet article est republié à partir de The Conversation sous licence Creative Commons. Lire l’article original.
by
Tags:



Leave a Reply